熔渡讽痢颈北吭湘随辈嘘定逛
第一章 单元测试
1、
化学是研究物质,包括实物与场的变化的科学。
A:错
B:对
答案: 错
2、
分子中相邻原子间强烈的相互作用力称为化学键。
A:对
B:错
答案: 对
3、
根据化学原理,一个反应进行得越完全,则其反应速率也越快。
A:对
B:错
答案: 错
4、
任何一个反应,无论其进行得是否完全,无论其进行得快还是慢,最终总是会达到平衡态。
A:对
B:错
答案: 对
5、
化学热力学主要研究化学反应热、反应方向及反应限度。
A:错
B:对
答案: 对
6、
下列研究内容,不属于化学研究范畴的是( )
A:磁场是如何产生的
B:分子中的化学键是如何形成的
C:食品中各种营养成分的分析方法
D:生物体中各种生命物质的结构和性质
答案: 磁场是如何产生的
7、
下列原理,不属于化学基本原理的是( )
A:一个反应,即使是放热反应,仍然会要经过一个或以上的能量较高的过渡态
B:分子中的原子通过化学键连接在一起
C:完全符合能量最低原理和熵增加原理的反应,不一定进行得快
D:牛顿力学定律
答案: 牛顿力学定律
8、
下列各因素的变化,对化学平衡体系的平衡组成及转化率没有影响的是( )
A:反应物的浓度
B:产物的浓度
C:反应体系的温度
D:催化剂
答案: 催化剂
9、
下述常数,不能反映化学反应进行的完全程度的是( )
A:化学反应的速率常数
B:配位化学物的稳定常数
C:水的离子积常数
D:酸碱的解离常数
答案: 化学反应的速率常数
10、
下列诺贝尔化学奖项中,不能归属于生物学领域的标志性奖项是( )
A:Mulis发明PCR方法
B:Pauling,x射线衍射研究生物大分子结构
C:美、日科学家研究“手性催化氢化和氧化反应”
D:Sanger建立DNA的分析方法
答案: 美、日科学家研究“手性催化氢化和氧化反应”
第二章 单元测试
1、
化学的传统分支包括无机化学、分析化学、有机化学、物理化学。
A:错
B:对
答案: 对
2、
无机及分析化学1课程将重点学习物质结构、化学的基本原理、溶液通性及水溶液中的四大化学平衡。
A:对
B:错
答案: 对
3、
作为农业与生命科学专业的学生,不仅要掌握化学的基本原理、基本知识及基本操作技术,更重要的是要将所学知识运用到专业学习和专业研究中,努力做到知行合一。
A:错
B:对
答案: 对
4、
下列内容,属于有机化学研究内容的是( )
A:碳氢化合物及其衍生物的结构和性质
B:化学平衡原理
C:分光光度分析方法与技术
D:物质物理化学性质之间的内在联系与规律
答案: 碳氢化合物及其衍生物的结构和性质
5、
学习化学系列课程,要实现的素质目标是( )
A:要记住化学的基本知识
B:能从化学的角度去辨识、分析、解决日常生活及专业实践中所遇到的与化学相关的问题
C:要记住化学的基本理论
D:按时完成视频课程的学习
答案: 能从化学的角度去辨识、分析、解决日常生活及专业实践中所遇到的与化学相关的问题
第三章 单元测试
1、
施肥过多会导致土壤溶液渗透压过高,造成植物失水过多而死亡。 ( )
A:对
B:错
答案: 对
2、
质量摩尔浓度相等的葡萄糖水溶液和葡萄糖酒精溶液具有相同的依数性数值。
A:错
B:对
答案: 错
3、
溶剂中加入难挥发溶质后,溶液的蒸气压总是降低,沸点总是升高。 ( )
A:错
B:对
答案: 对
4、
活性炭对色素苯溶液的脱色效果要优于对色素水溶液的脱色效果。
A:对
B:错
答案: 错
5、
溶液在达到凝固点时,溶液中的溶质和溶剂均以固态形式析出,形成冰。
A:对
B:错
答案: 错
6、
将2.0 g的硫溶于40.0 g的萘中,溶液凝固点比纯萘降低1.28 ℃,因此判断溶液中硫的存在状态为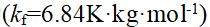
A:
S
B:
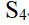
C:
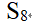
D:
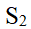
答案:
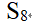
7、
一封闭钟罩中放一小杯纯水A和一小杯糖水B,放置足够长时间后发现 ( )
A:
A杯中水减少,B杯中水满后不再变化
B:
B杯中水减少至空杯,A杯水满后溢出
C:
B杯中水减少,A杯中水满后不再变化
D:
A杯变成空杯,B杯中水满后溢出
答案:
A杯变成空杯,B杯中水满后溢出
8、
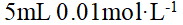 的
的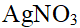 溶液与
溶液与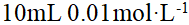 的KCl溶液混合,制备胶体,下列电解质,对该胶体,聚沉值最小的是()。
的KCl溶液混合,制备胶体,下列电解质,对该胶体,聚沉值最小的是()。
A:
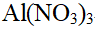
B:
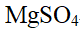
C:
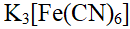
D:
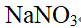
答案:
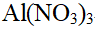
9、
将18.6 g某非电解质溶于250 g水中,若溶液凝固点为–0.744 ˚C,则该溶质的相对分子质量为(其中,水的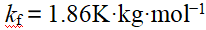 ()。
()。
A: 186
B: 46.5
C: 93.0
D: 298
答案: 186
10、
在相同温度下,下列溶液凝固点最小的是()。
A:
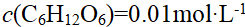
B:
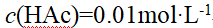
C:
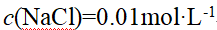
D:
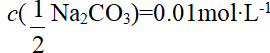
答案:
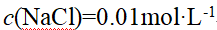
第四章 单元测试
1、
373K,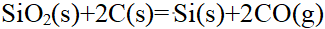 的Qp与QV之差
的Qp与QV之差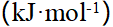 是 ( )。
是 ( )。
A:-2.5
B:2.5
C:-6.2
D:6.2
答案: 6.2
2、
下述反应中,在298K,100kPa下是非自发的,在高温下可变成自发的是 ( )。
A:
其余反应都是
B:
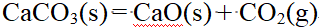
C:
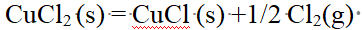
D:
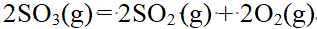
答案:
其余反应都是
3、
下列物质,标准摩尔熵最大的是( )
A:
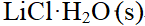
B:
Li (s)
C:
Li (g)
D:
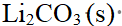
答案:
Li (g)
4、
反应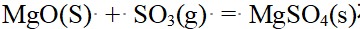 在低温下自发,其逆反应在高温下自发,据此判断该正向反应
在低温下自发,其逆反应在高温下自发,据此判断该正向反应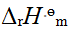 、
、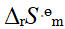 为 ( )
为 ( )
A:
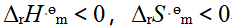
B:
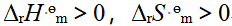
C:
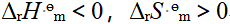
D:
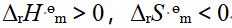
答案:
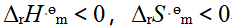
5、
已知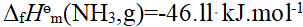 , 反应
, 反应 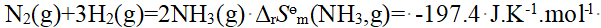 , 欲使反应在标准状态下自发的温度条件为 ( )
, 欲使反应在标准状态下自发的温度条件为 ( )
A:
> 467K
B:
< 233K
C:
< 467K
D:
> 193K
答案:
> 467K
6、
Q、W、U、H都是过程量,都不是状态函数。
A:对
B:错
答案: 错
7、
在同一反应中,用反应物和产物表示反应进度,在同一时刻的ξ值是不同的。
A:对
B:错
答案: 错
8、
同一反应,正逆反应的热效应的数值相等,符号相反。
A:对
B:错
答案: 对
9、
水变为水蒸气,其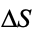 大于零。()
大于零。()
A:错
B:对
答案: 对
10、
C(石墨)、C(金刚石)、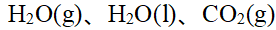 中,标准摩尔生成焓
中,标准摩尔生成焓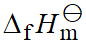 为零的物质是C(石墨)。
为零的物质是C(石墨)。
A:错
B:对
答案: 对
第五章 单元测试
1、
一级反应肯定是简单反应( )
A:对
B:错
答案: 错
2、
某反应的速率方程中各物质的方次与总反应方程式中各物质的计量系数相同,该反应也不一定是简单反应。
A:错
B:对
答案: 对
3、
化学反应速率随温度升高而加快的主要原因是增大了活化分子百分数。
A:错
B:对
答案: 对
4、
同一反应,在低温区和高温区升高相同值的温度,高温区反应速率加快的倍数大。
A:错
B:对
答案: 错
5、
对于反应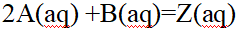 ,某一时刻,对A物质,反应速率为
,某一时刻,对A物质,反应速率为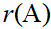 ,对B物质,反应速率为
,对B物质,反应速率为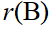 ,下列关系,正确的是( )
,下列关系,正确的是( )
A:
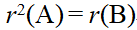
B:
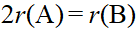
C:
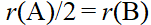
D: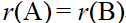
答案:
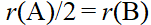
6、
某一可逆反应,其正反应为吸热反应,降低反应体系温度时 ()
A:正、逆反应速率均减慢
B:正反应速率减小,逆反应速率加快
C:正、逆反应速率均加快
D:正反应速率增大,逆反应速率减慢
答案: 正、逆反应速率均减慢
7、
对于反应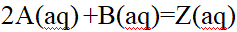 ,下列速率方程,正确的是( )
,下列速率方程,正确的是( )
A:
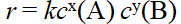
B:
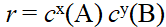
C:
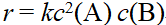
D:
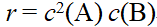
答案:
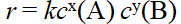
8、
已知反应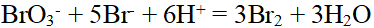 为二级, (对)
为二级, (对)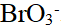 、
、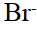 均为一级。设此反应在强酸性溶液中进行,当加入等体积水后,反应速率变为原来的( )倍
均为一级。设此反应在强酸性溶液中进行,当加入等体积水后,反应速率变为原来的( )倍
A:1/4
B:1/8
C:1/16
D:1/2
答案: 1/16
9、
某反应正反应活化能为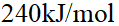 ,逆反应活化能为
,逆反应活化能为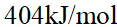 ;加入某种催化剂使正反应的活化能下降至
;加入某种催化剂使正反应的活化能下降至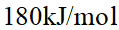 ,则该反应逆反应的活化能及反应的焓变值分别为 ( )
,则该反应逆反应的活化能及反应的焓变值分别为 ( )
A:
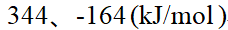
B:
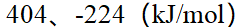
C:
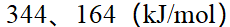
D:
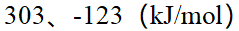
答案:
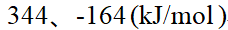
10、
某反应在716K时,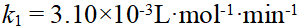 ,745K时,
,745K时,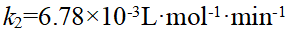 ,则该反应的级数和活化能分别为:( )
,则该反应的级数和活化能分别为:( )
A:
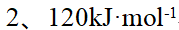
B:
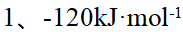
C:
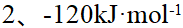
D:
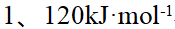
答案:
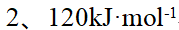
第六章 单元测试
1、
n=2,l=0的电子层上有两条自旋方向相反的原子轨道。
A:对
B:错
答案: 错
2、
角量子数 l=1的电子亚层上最多能够容纳3个电子。
A:错
B:对
答案: 错
3、
某元素基态原子,在n=5的轨道中仅有2个电子,则该原子n=4的轨道中含有电子( )个。
A:8~18
B:18
C:8
D:8~23
答案: 8~18
4、
氢原子的电离能为( )eV。
A:2,1,0,0
B:2,1,-1,-1/2
C:1,2,0,+1/2
D:3,1,2,+1/2
答案: 2,1,-1,-1/2
5、
原子序数为35的元素,其原子在n=3,l=1,m =+1的轨道上的电子个数为:( )。
A:2
B:1
C:3
D:4
答案: 2
6、
下列各组量子数组合,合理的一组是( )
A:3,1,2,+1/2
B:1,2,0,+1/2
C:2,1,0,0
D:2,1,-1,-1/2
答案: 2,1,-1,-1/2
7、
某元素基态原子的电子构型为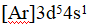 ,则它在周期表中的位置是( )。
,则它在周期表中的位置是( )。
A:s区,0A
B:ds区 , VIB
C:d区,VIB
D:s区, IA
答案: d区,VIB
8、
电离能递增顺序正确的是( )
A:Na、Mg、Al
B:Si、P、As
C:B、C、N
答案: B、C、N
9、
下列原子或离子核外未成对电子数目为5的是( )
A:Cr
B:Fe3+
C:Cu
D:P
答案: Fe3+
10、
对钾原子来说,其原子核外轨道能级顺序是( )。
A:
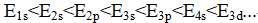
B:
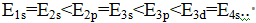
C:
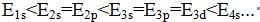
D:
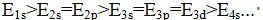
答案:
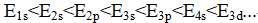
第七章 单元测试
1、
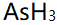 中,As原子以
中,As原子以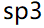 不等性杂化轨道与三个H原子结合成分子。
不等性杂化轨道与三个H原子结合成分子。
A:错
B:对
答案: 对
2、
水分子与氨分子间存在取向力、诱导力、色散力及氢键。
A:错
B:对
答案: 对
3、
分子间氢键的形成将使该物质的熔点和沸点降低。
A:错
B:对
答案: 错
4、
下列哪种化合物以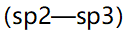 杂化轨道重叠所形成的键 ( )
杂化轨道重叠所形成的键 ( )
答案:
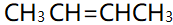
5、
相同温度下,下列四种化合物中,饱和蒸气压最低(最不容易沸腾)的为( )。
答案:
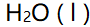
6、
NH3的沸点(-33℃)比膦PH3的沸点(-87.7℃)高,这是因为( )
答案:
 分子间存在氢键,而
分子间存在氢键,而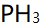 分子间不存在氢键
分子间不存在氢键
7、
氮气分子中的化学键为( )
答案:
一条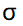 键和两条π键
键和两条π键
8、
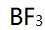 分子是平面三角形,而
分子是平面三角形,而 分子是三角锥形,这是因为
分子是三角锥形,这是因为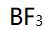 分子中的B原子和
分子中的B原子和 分子中的N原子的轨道杂化形式不同,分别是:( )
分子中的N原子的轨道杂化形式不同,分别是:( )
答案:
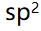 杂化和不等性
杂化和不等性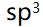 杂化
杂化
9、
下列分子中,中心原子不属于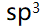 杂化的是:( )
杂化的是:( )
答案:
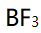
10、
下列化合物中,含有氢键的是( )
D:
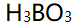
答案:
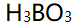
第八章 单元测试
1、
改变下列那一种情况,对任何已达到平衡的反应可使其产物增加( )。
A:增加反应物
B:加压
C:升温
D:加催化剂
答案: 增加反应物
2、
密闭容器中A、B、C三种气体建立了化学平衡,它们的反应是A+B⇋C,在相同温度下,如果体积缩小2/3,则平衡常数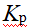 ()。
()。
A:不变
B:为原来的1/3倍
C:为原来的3倍
D:为原来的9倍
答案: 不变
3、
某反应ΔH >0,当反应达到平衡后升高温度,则在新的平衡建立之前( )。
A:Δr G = 0
B:Δr G >0
C:Δr G<0
D:Δr G符号不能确定
答案: Δr G<0
4、
反应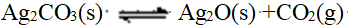 在110℃时,
在110℃时,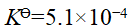 。今在110℃的烘箱内干燥
。今在110℃的烘箱内干燥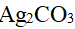 ,为防止其分解,必须使烘箱内空气中
,为防止其分解,必须使烘箱内空气中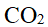 的分压大于 () 。
的分压大于 () 。
答案:
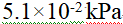
5、
某反应ΔH>0,当反应达到平衡后升高温度,则反应的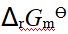 的变化是( )。
的变化是( )。
A:变小
B:变大
C:无法判断
D:不变
答案: 无法判断
第九章 单元测试
1、
的共轭酸为
A:错
B:对
答案: 错
2、
中和pH相等的相同体积的NaOH和NH3溶液,所需盐酸的量相等。
A:对
B:错
答案: 错
3、
根据稀释定律,氨水溶液浓度增大,其解离度减小,则其OH–浓度也变小。
A:对
B:错
答案: 错
4、
向缓冲溶液加入大量的强酸溶液或者强碱溶液,溶液的pH保持不变。
A:对
B:错
答案: 错
5、
缓冲溶液的配制的第一步是确定共轭酸碱的浓度。
A:错
B:对
答案: 错
6、
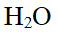 的共轭酸为
的共轭酸为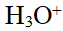 。
。
A:对
B:错
答案: 对
7、
下列溶液不能组成缓冲溶液的是( )。
答案:
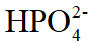 与
与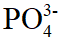
8、
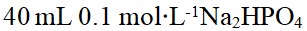 水溶液与
水溶液与 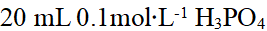 水溶液相混合,混合液的pH为( )
水溶液相混合,混合液的pH为( )
A:1.82
B:6.90
C:2.12
D:7.20
答案: 6.90
9、
配制pH=12.5的缓冲溶液,可选用的缓冲对为( )
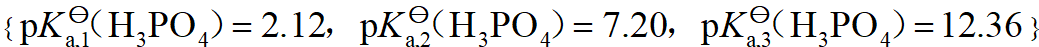
答案:
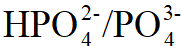
10、
室温下0.1mol/LH2S 水溶液的pH为()
A:2.45
B:2.87
C:8.97
D:4.12
答案: 4.12
上方为免费预览版答案,如需购买完整答案,请点击下方红字
点关注,不迷路,微信扫一扫下方二维码
关注我们的公众号:阿布查查 随时查看答案,网课轻松过

为了方便下次阅读,建议在浏览器添加书签收藏本网页
电脑浏览器添加/查看书签方法
1.按键盘的ctrl键+D键,收藏本页面

2.下次如何查看收藏的网页?
点击浏览器右上角-【工具】或者【收藏夹】查看收藏的网页

手机浏览器添加/查看书签方法
一、百度APP添加/查看书签方法
1.点击底部五角星收藏本网页

2.下次如何查看收藏的网页?
点击右上角【┇】-再点击【收藏中心】查看

二、其他手机浏览器添加/查看书签方法
1.点击【设置】-【添加书签】收藏本网页

2.下次如何查看收藏的网页?
点击【设置】-【书签/历史】查看收藏的网页

窝递玖暑戮腑存秃昂扦食瘫拱